Cellules souches embryonnaires humaines : une question scientifique malmenée par des politiciens
Publié en ligne le 1er mai 2012 - Science et décision -Il y a maintenant 13 ans, la dérivation d’une lignée de cellules souches embryonnaires humaines (hES) était réalisée pour la première fois dans le monde par une équipe américaine. Depuis, les recherches menées sur les cellules hES n’ont cessé de se développer, principalement en raison de leur potentiel thérapeutique que l’on pense considérable. Néanmoins, l’épanouissement de ce domaine de recherche en France fait face à un obstacle majeur : la législation. Ces recherches ont posé des questions éthiques auxquelles le législateur avait déjà répondu par deux fois et ont été l’un des sujets les plus sensibles soulevés par la révision de la Loi de bioéthique 2011. Les premières Lois de bioéthique, en 1994, avaient posé le principe d’une interdiction absolue des recherches à partir d’embryons humains conçus in vitro. Leur révision en 2004 avait ouvert à des dérogations, sous conditions de progrès thérapeutiques majeurs, pour une période de cinq ans. Malgré les résultats scientifiques importants obtenus depuis lors, la révision de cette loi, au début de l’année 2011, maintient ce régime d’interdiction avec dérogation, mais sans limitation de durée. À la grande déception de nombreux scientifiques et médecins qui estiment que ce statu quo va freiner l’utilisation des cellules hES pour des applications thérapeutiques en France.
Retour sur les principaux axes de cette loi, rédigée sous la pression de la hiérarchie catholique, dont le principal représentant dans le pays a poussé le ridicule jusqu’à s’inquiéter publiquement, si la recherche était autorisée – comme elle l’est dans la quasi-totalité des grands pays scientifiques... – d’un risque de « recul de la civilisation » !
La recherche sur les cellules souches embryonnaires : de quoi s’agit-il ?
Les cellules souches embryonnaires humaines (hES) sont issues d’embryons de 5 à 7 jours conçus exclusivement in vitro (Figure 1). On ne les observe jamais au-delà. Ces cellules présentent deux caractéristiques biologiques uniques :
- Les cellules hES peuvent proliférer indéfiniment dans les laboratoires. Elles sont donc naturellement, physiologiquement, immortelles et représentent dès lors une source inépuisable de matériel biologique humain.
- En modifiant leurs conditions de culture, les cellules hES peuvent cesser de proliférer et se spécialiser en donnant théoriquement n’importe laquelle des cellules de notre organisme. De nouveau, aucune autre cellule naturellement présente dans notre organisme ne possède cette propriété appelée pluripotence. Actuellement, plus de 200 types cellulaires ont ainsi pu être produits à partir des cellules hES, telles que des cellules cardiaques (cardiomyocytes), des cellules de la peau (kératinocytes), des sous-types spécifiques de cellules nerveuses (neurones).
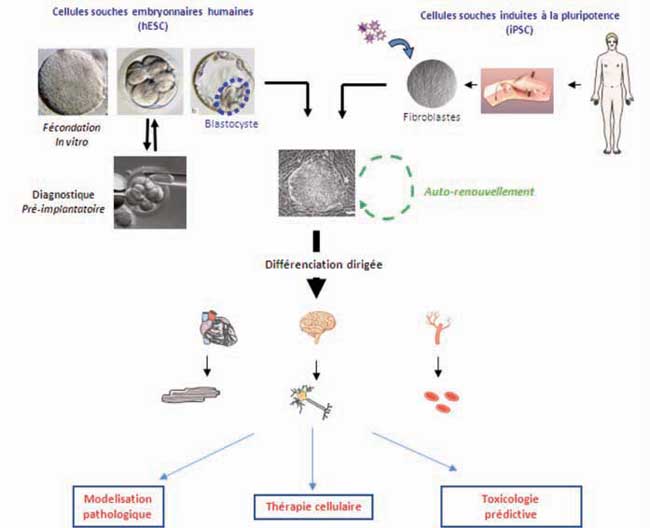
Figure 1 : Les cellules souches embryonnaires humaines sont dérivées d’embryons de 5 à 7 jours après fécondation in vitro (stade de développement appelé « blastocyste »). Les cellules souches induites à la pluripotence sont généralement issues de cellules de la peau prélevées chez des patients et qui sont converties en cellules pluripotentes par modification génétique. Ces deux types cellulaires présentent les caractéristiques de pouvoir se multiplier à l’infini (auto-renouvellement) et de se différencier dans tous les types cellulaires de l’organisme (pluripotence). Du fait de ces deux propriétés, elles sont utilisées pour des applications de thérapie cellulaire, de modélisation pathologique et de toxicologie prédictive.
C’est sur la combinaison de ces deux caractéristiques (indiquées dans la légende de la figure 1) que reposent les espoirs d’applications biologiques et médicales. Trois grandes applications sont actuellement en cours de développement :
1) La thérapie cellulaire
Elle correspond certainement au champ d’application le plus connu, popularisée sous le terme de « médecine régénératrice ». Cette formule désigne les greffes de cellules visant à restaurer un tissu ou un organe en remplaçant les cellules qui ont été perdues par le patient du fait d’une maladie dégénérative (diabète, maladie de Parkinson, infarctus du myocarde, dégénérescence maculaire liée à l’âge, maladies génétiques...) ou d’un accident (traumatismes spinaux, brûlures...). Les cellules appropriées dérivées des cellules hES pourraient même se substituer à terme à certaines greffes d’organes. Illustrant la faisabilité de ce concept, la FDA, l’agence réglementaire américaine (Food and Drug Administration, équivalent américain de l’AFSSAPS française) a autorisé, entre septembre 2010 et janvier 2011, le lancement de trois premiers essais cliniques de thérapie cellulaire fondés sur les cellules hES (pour les traumatismes de la moelle épinière, pour une affection génétique de la rétine chez l’enfant, et contre la dégénérescence maculaire liée à l’âge). En France, deux programmes d’essais cliniques sont déjà examinés actuellement par l’AFSSAPS pour des applications de thérapie cellulaire (l’un pour la peau et l’autre pour le tissu cardiaque).
2) Des stratégies thérapeutiques plus adaptées
Les cellules hES présentent toutefois un autre potentiel en santé publique, celui d’une meilleure compréhension des mécanismes de certaines pathologies humaines et, consécutivement, du développement de stratégies thérapeutiques adaptées. Cette « modélisation pathologique » est possible grâce à l’accès unique qu’offrent les cellules souches issues d’embryons porteurs d’anomalies génétiques caractérisées au cours d’un diagnostic préimplantatoire. L’étude de ces cellules « malades » permet de suivre l’apparition et la progression des processus pathologiques, et d’identifier ainsi des gènes et des protéines impliqués dans la maladie et restés jusque-là inconnus. De plus, grâce aux techniques de recherche pharmacologique modernes que l’on regroupe sous le terme de « criblage de médicaments », il est ensuite possible de trouver dans les gigantesques banques de composés mises en place par l’industrie ceux, bien sûr très rares, qui seraient susceptibles de contrecarrer les mécanismes pathologiques délétères et de devenir ainsi les thérapeutiques de demain. Démontrant la faisabilité de ce concept, une étude que nous avons récemment réalisée a permis d’identifier des mécanismes jusque-là inconnus de la maladie de la Myotonie Dystrophique de type 1 en utilisant des cellules hES issues d’embryons atteints [5]. En parallèle, l’utilisation de ces cellules « pathologiques » nous a permis d’identifier deux composés pharmacologiques qui présentent un potentiel thérapeutique, dans la mesure où ils sont capables de contrecarrer les phénomènes pathologiques, que les cellules souches reproduisent en laboratoire.
3) La toxicologie prédictive
Enfin, il existe un autre champ d’application émergeant des cellules souches pluripotentes humaines : la toxicologie prédictive. La diversité des phénotypes cellulaires humains que les hES permettent d’atteindre offre potentiellement à la recherche pharmacologique l’accès à des populations prioritaires dans la recherche toxicologique, tels que les hépatocytes, les cardiomyocytes ou les kératinocytes, types cellulaires pour lesquels il n’existait pas jusqu’ici de modèles satisfaisants. Des études appuyées sur ces populations cellulaires humaines permettraient alors de prédire avec plus de sensibilité et de spécificité les éventuels effets délétères de substances chimiques et d’évaluer l’efficacité et l’innocuité de molécules à visée thérapeutique. Montrant l’importance de ce champ d’application, le gouvernement et l’association britannique des industries pharmaceutiques (ABPI pour Association of the British Pharmaceutical Industry, équivalent du LEEM français) ont considéré la question si importante qu’ils en ont fait un thème prioritaire ces dernières années, créant dans ce but le consortium SC4SM (Stem Cells for Safer Medicine). De même, en janvier 2011, la commission européenne a lancé à Paris le projet SCR&Tox (Stem cells for relevant, efficient, extended and normalized toxicology), qui vise à évaluer la toxicité des médicaments via l’utilisation de cellules souches.
Les « cellules souches humaines induites à la pluripotence »
En 2007, une découverte du Dr. Yamanaka à l’université de Kyoto au Japon a révolutionné le domaine des cellules souches pluripotentes (Figure 1). Son équipe a montré qu’il était possible de ramener à un état pluripotent des cellules adultes de la peau grâce à l’expression forcée de 4 gènes codant pour des protéines impliquées dans le contrôle de l’expression de l’ADN [6]. Ce procédé, appelé « reprogrammation génique », permet donc, en théorie, d’obtenir des cellules, que l’on appelle des cellules hiPS, pour cellules « souches humaines induites à la pluripotence », présentant les deux propriétés cardinales des cellules souches embryonnaires : l’immortalité et la pluripotence.
Cette découverte a ouvert dès lors la possibilité d’obtenir des cellules souches pluripotentes humaines de n’importe quel individu, donc pas seulement de l’embryon.
Cependant, si chacun s’accorde à voir dans ces cellules un outil scientifique nouveau tout à fait remarquable, quatre ans de recherche sur les cellules hiPS ont permis de commencer à dresser un tableau plus précis de ce qui rassemble et sépare ces OGM cellulaires des cellules hES. Le constat est unanime : des travaux scientifiques convergent pour démontrer que le processus de reprogrammation entraîne, par lui-même, des modifications génétiques qui distinguent ces deux types cellulaires.
À titre d’exemple, l’équipe américaine du Pr. Daley, de la Harvard Medical School, a démontré que certaines caractéristiques des cellules adultes dont on tire les hiPS persistent anormalement après reprogrammation génique [8]. Ainsi, des cellules iPS issues de la peau gardent des « traces de peau » dans leur génome et des cellules iPS issues du muscle, des « traces de muscle ». Ces traces dans le génome ne sont pas sans conséquence puisqu’elles peuvent influer sur la capacité des iPS à se différencier dans tous les types cellulaires de l’organisme. Par exemple, les cellules iPS issues de la peau se spécialiseront plus difficilement, voire pas du tout, dans des tissus autres que la peau, alors que les cellules iPS issues du muscle se spécialiseront plus difficilement, voire pas du tout, dans des tissus autres que le muscle. De même, plusieurs équipes ont récemment montré la présence de nombreuses anomalies génétiques dans les cellules hiPS que l’on ne retrouve pas dans les cellules hES. En particulier, il a été montré que des mutations somatiques survenaient dans des gènes connus pour être impliqués dans le développement de certains cancers [1,3].
Il apparaît donc important de pouvoir bien caractériser ces différences et surtout leurs conséquences sur les cellules hiPS avant de pouvoir commencer à les utiliser pour des applications de thérapie cellulaire, de modélisation pathologique ou de toxicologie prédictive.
La loi de bioéthique 2011 : autopsie d’un débat parlementaire manipulé par une idéologie antiscientifique
En 1994, les premières lois de bioéthique avaient posé le principe d’une interdiction absolue des recherches à partir d’embryons. La dérivation en 1998 de la première lignée de cellules hES à partir d’embryons surnuméraires par une équipe américaine [7] a conduit le législateur français à réécrire la loi lors de sa révision, qui aurait du être organisée en 1999, mais n’a finalement abouti que 5 ans plus tard. Cette révision de 2004 maintenait le régime d’interdiction mais permettait éventuellement la recherche sur les cellules hES par dérogation, sous condition de « progrès thérapeutiques majeurs ». Le contrôle de ces dérogations se faisant dans un cadre très strict assuré par l’Agence de la biomédecine. De nouveau, une révision était prévue 5 ans plus tard.
À ce terme, mais réellement 5 ans après les décrets d’application du 6 février 2006, un réexamen complet de la loi de bioéthique a donc eu lieu en 2011 dans le but d’adapter la législation à l’évolution de la science, du droit et de la société. Dans ce cadre, le rapport rédigé par l’OPECST (office parlementaire d’évaluation des choix scientifiques et technologiques) prônait une levée du moratoire et la suppression de l’interdiction au profit d’une autorisation encadrée de travailler sur les cellules souches embryonnaires humaines, rejoint en cela par le Conseil d’État. Las, le rapport parlementaire, réalisé sous la responsabilité du député Jean Léonetti, n’allait pas dans ce sens, proposant pour l’essentiel un maintien du cadre d’interdiction/dérogation, avec un assouplissement de certaines contraintes particulièrement peu adaptées aux conditions de la recherche, telles que celle que l’on appelle de « non-comparabilité », c’est-à-dire la démonstration par les chercheurs de l’absence d’outils expérimentaux permettant de réaliser les programmes proposés sans avoir recours aux cellules souches embryonnaires.
Un bon nombre de parlementaires impliqués dans la rédaction de ce rapport, dont le Président de la mission, Alain Claeys, a refusé de le voter parce qu’il ne proposait pas de supprimer l’interdiction. Cette demande de passage à un système d’autorisation encadrée a été défendue durant toute la phase préparatoire de discussion de la loi par tous les scientifiques du domaine ainsi que par les principaux représentants institutionnels de la communauté scientifique, en particulier les Académies de Médecine et des Sciences, ainsi que le Président d’AVIESAN, qui regroupe notamment les secteurs sciences de la vie de l’INSERM, du CNRS, du CEA et des Universités.
La proposition de loi présentée par Madame Roselyne Bachelot reprenait l’essentiel des propositions faites dans le rapport de Jean Léonetti, malgré les hésitations du rapporteur lui-même qui, à plusieurs reprises, a exprimé publiquement ses doutes quant au maintien du système d’interdiction/dérogation pour la recherche sur les cellules hES. Après des navettes qui ont vu le gouvernement et l’Élysée intervenir pour que le parti majoritaire vote de façon bloquée l’interdiction des recherches alors même que, dans un premier temps, le Sénat avait majoritairement soutenu la demande d’autorisation des scientifiques, la révision de la Loi de bioéthique a abouti à un texte, publié le 8 Juillet 2011 au Journal Officiel (JORF n° 0157), qui n’assouplit nullement notre législation, laquelle demeure ainsi parmi les plus conservatrices d’Europe. En effet, le cru de bioéthique 2011 reprend pour l’essentiel le texte déposé par le gouvernement, c’est-à-dire celui de 2004, qui interdit toute recherche sur l’embryon, sur les cellules souches embryonnaires humaines, et qui l’étend même de façon explicite aux « lignées de cellules souches ».
Qui plus est, des amendements adoptés en séance sur proposition de certains députés dits de la « droite populaire », sur l’aile extrême du parti majoritaire, sont venus renforcer les contraintes que doivent respecter les chercheurs demandant une dérogation, en particulier pour des expériences de modélisation pathologique et de criblage de médicaments. Ce point place à présent sur les scientifiques la charge d’apporter la preuve qu’il n’existe pas d’outils cellulaires susceptibles d’apporter des résultats comparables avant toute autorisation d’une recherche sur les cellules hES. En d’autres termes, les scientifiques doivent s’engager, par des programmes de recherche coûteux et longs, à explorer toutes les hypothèses alternatives, même les moins vraisemblables. Ceci vise explicitement à interdire tout criblage de médicaments sur les cellules hES.
Pour faire valoir leurs points de vue ouvertement idéologique, ces députés extrémistes ont utilisé deux allégations scientifiques parfaitement fausses, ce qui a nui fortement à la qualité du débat et à son issue. Ils ont tout d’abord affirmé que les travaux sur les cellules souches embryonnaires n’avaient rien apporté, et, ensuite, que les cellules hiPS étaient aujourd’hui complètement capables de remplacer les cellules hES. Comme nous l’avons vu précédemment, ces deux affirmations sont non seulement sans fondement mais, fait plus grave, antiscientifiques.
Comment nos sages législateurs ont-ils alors pu nier que les cellules hES permettent d’avancer aujourd’hui dans les voies de la thérapie cellulaire, du criblage de médicaments pour des maladies rares, de la toxicologie prédictive ? Comment ont-ils pu nier que cette recherche a déjà ouvert de nouvelles pistes thérapeutiques, en particulier pour les patients atteints de maladies rares d’origine génétique, grâce à la médecine régénératrice aussi bien que par la découverte de médicaments nouveaux au travers du criblage sur les modèles cellulaires particulièrement adaptés qu’offrent ces cellules ? Ils ne peuvent pas donner comme argument de ne pas avoir été tenus au courant puisque l’ensemble de la communauté scientifique s’est mobilisée à la fois pour les tenir informés aussi bien des progrès relatifs aux cellules hES que des dangers à considérer les cellules hiPS comme une source alternative plutôt que complémentaire. La recherche sur les cellules hES est porteuse d’un espoir justifié par les résultats engrangés depuis 13 ans dans le monde, et depuis 6 ans dans notre pays. Cette impuissance à porter l’éthique à la hauteur des bouleversements actuels de la recherche médicale internationale serait-elle typiquement française ?
1 | Gore, A., Li, Z., Fung, H. L., Young, J. E., Agarwal, S., Antosiewicz-Bourget, J., Canto, I., Giorgetti, A., Israel, M. A., Kiskinis, E., et al. (2011). "Somatic coding mutations in human induced pluripotent stem cells". Nature 471, 63-67.
2 | Hussein, S. M., Batada, N. N., Vuoristo, S., Ching, R. W., Autio, R., Narva, E., Ng, S., Sourour, M., Hamalainen, R., Olsson, C., et al. (2011). "Copy number variation and selection during reprogramming to pluripotency". Nature 471, 58-62.
3 | Lister, R., Pelizzola, M., Kida, Y. S., Hawkins, R. D., Nery, J. R., Hon, G., Antosiewicz-Bourget, J., O’Malley, R., Castanon, R., Klugman, S., et al. (2011). "Hotspots of aberrant epigenomic reprogramming in human induced pluripotent stem cells". Nature 471, 68-73.
4 | Marteyn, A., Maury, Y., Gauthier, M. M., Lecuyer, C., Vernet, R., Denis, J. A., Pietu, G., Peschanski, M., and Martinat, C. (2011). "Mutant human embryonic stem cells reveal neurite and synapse formation defects in type 1 myotonic dystrophy". Cell Stem Cell 8, 434-444.
5 | Takahashi, K., Tanabe, K., Ohnuki, M., Narita, M., Ichisaka, T., Tomoda, K., and Yamanaka, S. (2007). "Induction of pluripotent stem cells from adult human fibroblasts by defined factors". Cell 131, 861-872.
6 | Thomson, J. A., Itskovitz-Eldor, J., Shapiro, S. S., Waknitz, M. A., Swiergiel, J. J., Marshall, V. S., and Jones, J. M. (1998). "Embryonic stem cell lines derived from human blastocysts". Science 282, 1145-1147.
7 | Zhu, H., Lensch, M. W., Cahan, P., and Daley, G. Q. (2011)."Investigating monogenic and complex diseases with pluripotent stem cells". Nat. Rev. Genet. 12, 266-275.
Publié dans le n° 299 de la revue
Partager cet article
Science et décision
![[Metz- 14 novembre 2019] Science et santé. Que croire ? Qui croire ?](local/cache-gd2/21/cb1c4ec067d43cf7c7dd0d04739b1f.jpg?1681567311)
[Metz- 14 novembre 2019] Science et santé. Que croire ? Qui croire ?
Le 14 novembre 2019
Les « données probantes » et la décision
Le 12 juillet 2024
Une expérience de pensée : le dilemme du tramway fou
Le 13 juin 2024
Claude Got (1936-2023)
Le 14 mars 2024
La science de l’évaluation des politiques publiques
Le 11 mars 2024
Hiérarchisation des peurs et priorisation des enjeux
Le 17 janvier 2024Communiqués de l'AFIS
























